Centro nazionale Malattie Rare

TELEFONO VERDE MALATTIE RARE
Servizio nazionale di informazione e orientamento per cittadini e professionisti nell’ambito dei percorsi, delle iniziative e delle risorse relativi alle malattie rare, attraverso la metodologia del counseling telefonico
REGISTRO NAZIONALE MALATTIE RARE
Strumento scientifico-istituzionale per la sorveglianza delle malattie rare (MR)
CONTROLLO ESTERNO DI QUALITA'
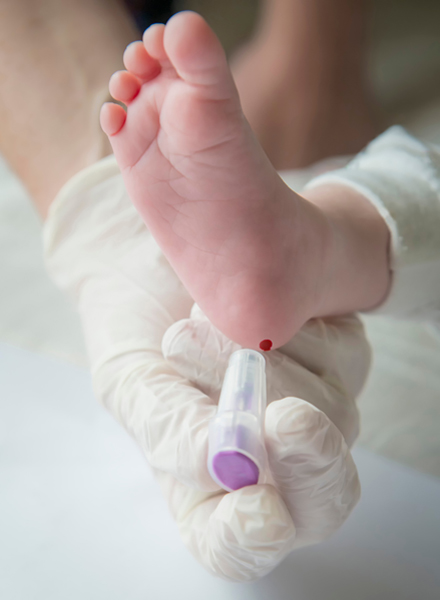
Test genetici e test del sudore per fibrosi cistica